??? 8月12日�����,國(guó)家醫(yī)保局發(fā)出《關(guān)于公示通過2025年國(guó)家基本醫(yī)療保險(xiǎn)�、生育保險(xiǎn)和工傷保險(xiǎn)藥品目錄及商保創(chuàng)新藥目錄調(diào)整初步形式審查的藥品及相關(guān)信息的公告》��。
?? 據(jù)悉����,2025年7月11日至7月20日17時(shí),國(guó)家醫(yī)保局共收到基本醫(yī)保目錄申報(bào)信息718份�,涉及藥品通用名633個(gè)��,經(jīng)初步審核���,534個(gè)通過形式審查�����。其中目錄外申報(bào)信息472份����,涉及藥品通用名393個(gè)����,通過初審的通用名310個(gè),較2024年249個(gè)通過形式審查明顯增加�。
??? 國(guó)家醫(yī)保局共收到商保創(chuàng)新藥目錄申報(bào)信息141份����,涉及藥品通用名141個(gè)�,經(jīng)初步審核���,121個(gè)藥品通用名通過形式審查�����。
??? 初步形式審查的藥品名單及信息的公示時(shí)間為:2025年8月12日-8月18日�。公告顯示�,通過形式審查不等于納入基本醫(yī)保目錄或商保創(chuàng)新藥目錄��,后續(xù)還需要按程序開展專家評(píng)審����、談判競(jìng)價(jià)/價(jià)格協(xié)商等環(huán)節(jié)����。
附:國(guó)家醫(yī)保局解讀內(nèi)容
??? 根據(jù)2025年國(guó)家基本醫(yī)療保險(xiǎn)、生育保險(xiǎn)和工傷保險(xiǎn)藥品目錄和商業(yè)健康保險(xiǎn)創(chuàng)新藥品目錄(以下分別簡(jiǎn)稱基本醫(yī)保目錄和商保創(chuàng)新藥目錄)調(diào)整有關(guān)工作安排����,在相關(guān)部門的支持下�����,國(guó)家醫(yī)保局近期對(duì)申報(bào)藥品進(jìn)行了初步形式審查,并對(duì)通過初審的藥品名單和主要信息進(jìn)行公示?�,F(xiàn)就有關(guān)工作情況解讀如下:
??? 一、初步形式審查的作用和意義
??? 形式審查是對(duì)申報(bào)藥品是否符合當(dāng)年基本醫(yī)保目錄和商保創(chuàng)新藥目錄調(diào)整申報(bào)條件以及藥品信息完整性進(jìn)行的審核����。根據(jù)《2025年國(guó)家基本醫(yī)療保險(xiǎn)�����、生育保險(xiǎn)和工傷保險(xiǎn)藥品目錄及商業(yè)健康保險(xiǎn)創(chuàng)新藥品目錄調(diào)整工作方案》,形式審查分為初審��、初審結(jié)果公示����、復(fù)審、復(fù)審結(jié)果公告四個(gè)步驟�。本次公示的內(nèi)容即為今年的初審結(jié)果�����。
??? 通過對(duì)藥品申報(bào)資料進(jìn)行形式審查,一方面可以確保申報(bào)的藥品符合申報(bào)條件����,另一方面對(duì)申報(bào)資料的完整性����、規(guī)范性進(jìn)行審核,有利于后續(xù)評(píng)審���、測(cè)算階段相關(guān)信息的全面、真實(shí)���、準(zhǔn)確�。同時(shí),為確保目錄調(diào)整公開透明�,國(guó)家醫(yī)保局對(duì)通過初審的藥品名單和主要信息進(jìn)行公示���,本身也是主動(dòng)接受監(jiān)督的一種方式���,我們歡迎社會(huì)各界幫助我們發(fā)現(xiàn)問題,提出寶貴意見和建議��。
??? 二、通過初步形式審查是否意味著已被納入基本醫(yī)保目錄或商保創(chuàng)新藥目錄?
??? 按照《基本醫(yī)療保險(xiǎn)用藥管理暫行辦法》和《2025年國(guó)家基本醫(yī)療保險(xiǎn)��、生育保險(xiǎn)和工傷保險(xiǎn)藥品目錄及商業(yè)健康保險(xiǎn)創(chuàng)新藥品目錄調(diào)整工作方案》��,目錄調(diào)整分為企業(yè)申報(bào)����、形式審查���、專家評(píng)審��、談判競(jìng)價(jià)/價(jià)格協(xié)商等環(huán)節(jié),形式審查只是企業(yè)申報(bào)后目錄調(diào)整所有程序中的第一步���。
??? 一個(gè)藥品通過初步形式審查,只代表初審符合相應(yīng)申報(bào)條件���,還需要通過公示接受社會(huì)監(jiān)督,即使藥品最終確定通過形式審查��,也僅代表該藥品具備了參與目錄調(diào)整后續(xù)工作流程的資格�����,不代表其已經(jīng)納入了基本醫(yī)保目錄或商保創(chuàng)新藥目錄。
??? 三����、2025年企業(yè)申報(bào)和初步形式審查結(jié)果與去年相比有什么變化?
??? 2025年7月11日至7月20日17時(shí)���,國(guó)家醫(yī)保局共收到基本醫(yī)保目錄申報(bào)信息718份,涉及藥品通用名633個(gè)��,經(jīng)初步審核�,534個(gè)通過形式審查。其中目錄外申報(bào)信息472份�����,涉及藥品通用名393個(gè)��,通過初審的通用名310個(gè)����,較2024年249個(gè)通過形式審查明顯增加��。
??? 同時(shí),今年目錄調(diào)整中增設(shè)了商保創(chuàng)新藥目錄����,與基本醫(yī)保目錄同步申報(bào)����。國(guó)家醫(yī)保局共收到商保創(chuàng)新藥目錄申報(bào)信息141份�����,涉及藥品通用名141個(gè)�,經(jīng)初步審核,121個(gè)藥品通用名通過形式審查�����。
??? 有些藥品同時(shí)申報(bào)了基本醫(yī)保目錄和商保創(chuàng)新藥目錄�����,但因兩者申報(bào)條件不完全一致�,會(huì)出現(xiàn)基本醫(yī)保目錄和商保創(chuàng)新藥目錄形式審查結(jié)果不一致的情況�。
??? 四�、如何看待一些目前市場(chǎng)價(jià)格較為昂貴等明顯超出基本保障范圍的藥品通過了基本醫(yī)保目錄的形式審查?
??? 自成立以來��,國(guó)家醫(yī)保局堅(jiān)決貫徹黨中央�、國(guó)務(wù)院決策部署���,始終牢牢把握基本醫(yī)?����!氨����;尽钡墓δ芏ㄎ?�,堅(jiān)持盡力而為、量力而行�����,實(shí)事求是地確定保障范圍;始終堅(jiān)持穩(wěn)健可持續(xù)�����,將醫(yī)保基金和參保群眾的承受能力作為基本醫(yī)保目錄調(diào)整工作的基礎(chǔ)�����,通過準(zhǔn)入談判等方式大幅降低獨(dú)家藥品的價(jià)格;始終聚焦群眾基本醫(yī)療需求和臨床技術(shù)進(jìn)步間的平衡�,提升可及性,維護(hù)公平性�。
??? 有一些價(jià)格較為昂貴明顯超出基本醫(yī)保保障范圍的藥品通過了基本醫(yī)保目錄初步形式審查�����,僅表示該藥品符合申報(bào)條件�����,獲得了進(jìn)入下一個(gè)環(huán)節(jié)的資格���。這類藥品最終能否進(jìn)入基本醫(yī)保目錄�,還需要經(jīng)嚴(yán)格評(píng)審程序��,通過專家評(píng)審的獨(dú)家藥品談判成功��、非獨(dú)家藥品競(jìng)價(jià)成功才能最終納入目錄�����。
??? 五、本次公示后將進(jìn)行哪些工作?
??? 下一步�,我們將根據(jù)公示期間收到的反饋意見,對(duì)有關(guān)藥品信息進(jìn)行復(fù)核�,確定最終通過形式審查的藥品名單并向社會(huì)公布��。同時(shí)���,最終形式審查結(jié)果無論是否通過,均會(huì)通過2025 年基本醫(yī)保目錄及商保創(chuàng)新藥目錄調(diào)整申報(bào)模塊向申報(bào)企業(yè)反饋����。后續(xù),國(guó)家醫(yī)保局將按照工作方案要求��,抓緊推進(jìn)專家評(píng)審�、基本醫(yī)保目錄的談判競(jìng)價(jià)及商保創(chuàng)新藥目錄的價(jià)格協(xié)商等工作。
??? 感謝社會(huì)各界對(duì)醫(yī)療保障工作的關(guān)心和支持����。
2025版醫(yī)保藥品及商保創(chuàng)新藥目錄調(diào)整方案
??? 7月10日,國(guó)家醫(yī)保局正式公布《2025年國(guó)家基本醫(yī)療保險(xiǎn)�����、生育保險(xiǎn)和工傷保險(xiǎn)藥品目錄及商業(yè)健康保險(xiǎn)創(chuàng)新藥品目錄調(diào)整工作方案》等相關(guān)文件的公告 》
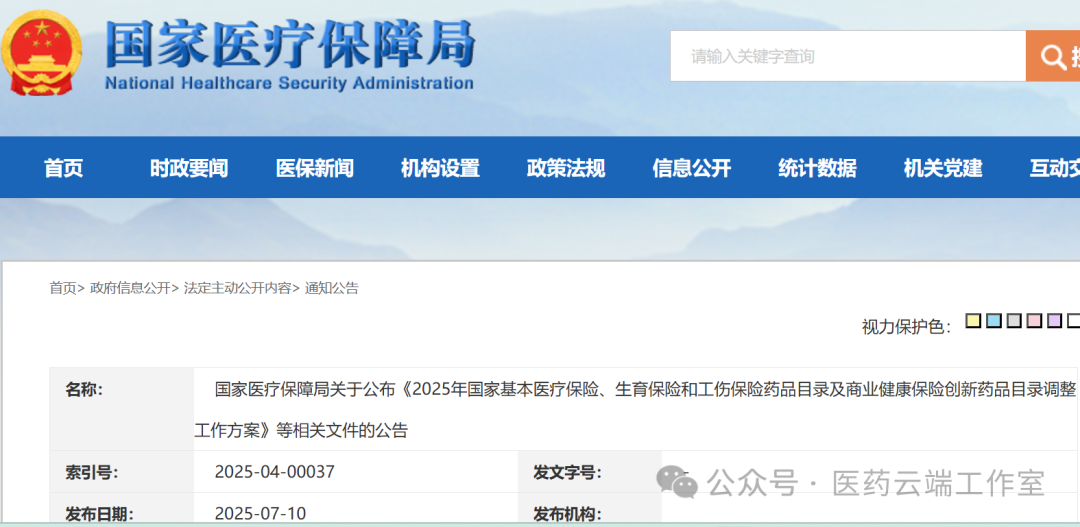
??? 目錄調(diào)整工作流程如下:
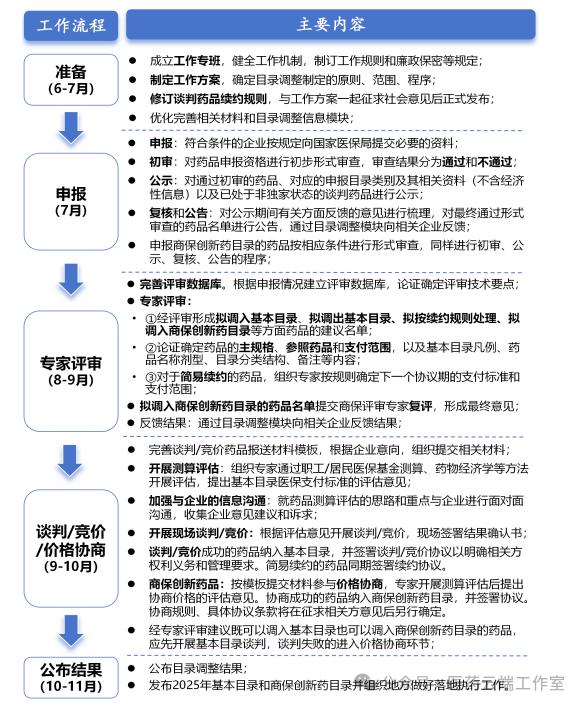

商保創(chuàng)新藥目錄申報(bào)全流程示意圖
??? 附:
??? 2025 年國(guó)家基本醫(yī)療保險(xiǎn)�、生育保險(xiǎn)和工傷保險(xiǎn)藥品目錄及商業(yè)健康保險(xiǎn)創(chuàng)新藥品目錄調(diào)整工作方案
??? 為貫徹落實(shí)黨中央����、國(guó)務(wù)院決策部署���,完善多層次醫(yī)療 保障體系,進(jìn)一步提高參保人員用藥保障水平�����,支持創(chuàng)新藥 和商業(yè)健康保險(xiǎn)高質(zhì)量發(fā)展,根據(jù)《中華人民共和國(guó)社會(huì)保 險(xiǎn)法》《基本醫(yī)療保險(xiǎn)用藥管理暫行辦法》等法律法規(guī)和國(guó) 家醫(yī)保局����、國(guó)家衛(wèi)生健康委《支持創(chuàng)新藥高質(zhì)量發(fā)展的若干 措施》等文件要求,現(xiàn)制定《2025 年國(guó)家基本醫(yī)療保險(xiǎn)���、生 育保險(xiǎn)和工傷保險(xiǎn)藥品目錄及商業(yè)健康保險(xiǎn)創(chuàng)新藥品目錄 調(diào)整工作方案》( 以下簡(jiǎn)稱《工作方案》)如下:
??? 一��、目標(biāo)任務(wù)
??? 以習(xí)近平新時(shí)代中國(guó)特色社會(huì)主義思想為指導(dǎo)�����,全面貫 徹黨的二十大和二十屆二中�、三中全會(huì)精神����,堅(jiān)持以人民健 康為中心,統(tǒng)籌考慮廣大參保人用藥保障需求�、基金支付能 力以及多層次醫(yī)療保障體系等因素���,開展 2025 年國(guó)家基本醫(yī) 療保險(xiǎn)��、生育保險(xiǎn)和工傷保險(xiǎn)藥品目錄( 以下簡(jiǎn)稱基本目錄) 調(diào)整,促進(jìn)目錄結(jié)構(gòu)更加合理優(yōu)化�、管理更加科學(xué)規(guī)范、支付更加管用高效�����、保障更加充分可及�。
??? 2025 年制定第一版商業(yè)健康保險(xiǎn)創(chuàng)新藥品目錄( 以下簡(jiǎn)稱商保創(chuàng)新藥目錄)���,主要納入超出保基本定位���、暫時(shí)無法納入基本目錄����,但創(chuàng)新程度高�、臨床價(jià)值大�、患者獲益顯著 的創(chuàng)新藥�����,推薦商業(yè)健康保險(xiǎn)、醫(yī)療互助等多層次醫(yī)療保障 體系參考使用����。
??? 二����、調(diào)整范圍
??? (一)基本目錄
??? 1. 目錄外西藥和中成藥
??? 符合《基本醫(yī)療保險(xiǎn)用藥管理暫行辦法》第七條���、第八 條規(guī)定,且具備以下情形之一的目錄外藥品��,可以申報(bào)納入 基本目錄( 乙類,下同 )���。
??? ( 1 )2020 年 1 月 1 日(含,下同)至 2025 年 6 月 30 日(含����,下同)期間,經(jīng)國(guó)家藥監(jiān)部門批準(zhǔn)上市的新通用名 藥品。
??? ( 2)2020 年 1 月 1 日至 2025 年 6 月 30 日期間���,經(jīng)國(guó) 家藥監(jiān)部門批準(zhǔn)�,適應(yīng)癥或功能主治發(fā)生重大變化��,且針對(duì) 此次變更獲得藥品批準(zhǔn)證明文件的藥品��。
??? ( 3)納入《國(guó)家基本藥物目錄( 2018 年版)》的藥品。
??? ( 4)納入鼓勵(lì)仿制藥品目錄或鼓勵(lì)研發(fā)申報(bào)兒童藥品清 單�����,且于 2025 年 6 月 30 日前��,經(jīng)國(guó)家藥監(jiān)部門批準(zhǔn)上市的 藥品�����。
??? ( 5)2025 年 6 月 30 日前�,經(jīng)國(guó)家藥監(jiān)部門批準(zhǔn)上市的 罕見病治療藥品。
??? 2. 目錄內(nèi)西藥和中成藥
??? ( 1)符合以下條件的應(yīng)申報(bào):
??? ①2025 年 12 月 31 日協(xié)議到期且不申請(qǐng)調(diào)整醫(yī)保支付范 圍的談判藥品���。
??? ②2025 年 12 月 31 日協(xié)議到期且適應(yīng)癥或功能主治未發(fā) 生重大變化, 因適應(yīng)癥或功能主治與醫(yī)保支付范圍不一致�, 主動(dòng)申請(qǐng)調(diào)整支付范圍的談判藥品�。
??? ③2020 年 1 月 1 日至 2025 年 6 月 30 日期間���,經(jīng)國(guó)家藥 監(jiān)部門批準(zhǔn),適應(yīng)癥或功能主治發(fā)生重大變化,主動(dòng)申請(qǐng)調(diào) 整醫(yī)保支付范圍的藥品����。
??? ( 2)具有以下情況之一的藥品將重點(diǎn)考慮調(diào)出基本目錄:
??? ①協(xié)議有效期內(nèi)未按約定保障市場(chǎng)供應(yīng)的談判藥品����。
??? ②近 3 年未向醫(yī)保定點(diǎn)醫(yī)藥機(jī)構(gòu)供應(yīng)或國(guó)家醫(yī)保信息平 臺(tái)上無交易量的常規(guī)目錄藥品。
??? ③符合《基本醫(yī)療保險(xiǎn)用藥管理暫行辦法》第九條����、第 十條規(guī)定的藥品。
??? 3.其他
??? ( 1)符合條件的中藥飲片納入調(diào)整范圍�����。
??? ( 2)完善基本目錄凡例�,規(guī)范藥品名稱劑型,適當(dāng)調(diào) 整藥品甲乙類別����、 目錄分類結(jié)構(gòu)、備注等內(nèi)容�。
??? ( 3)獨(dú)家藥品的認(rèn)定���、藥品說明書、價(jià)格費(fèi)用等以截 至 2025 年 6 月 30 日最新數(shù)據(jù)為準(zhǔn)���。
??? ( 二)商保創(chuàng)新藥目錄
??? 符合前述基本目錄外藥品申報(bào)條件( 1)或條件( 5 )的 獨(dú)家藥品,可以單獨(dú)申報(bào)商保創(chuàng)新藥目錄或同時(shí)申報(bào)商保創(chuàng) 新藥目錄����、基本目錄。
??? 三���、工作程序
??? 2025 年目錄調(diào)整分為準(zhǔn)備���、申報(bào)、專家評(píng)審��、談判��、公布結(jié)果 5 個(gè)階段����,基本目錄調(diào)整和商保創(chuàng)新藥目錄制定同步 進(jìn)行:
??? (一)準(zhǔn)備階段( 2025 年 6-7 月)
??? 1.組建工作機(jī)構(gòu),成立工作專班��,健全工作機(jī)制���,完善 專家?guī)欤朴喒ぷ饕?guī)則和廉政保密、利益回避等規(guī)定����。
??? 2.制定工作方案,確定目錄調(diào)整制定的原則��、范圍����、程序����,征求社會(huì)意見后正式發(fā)布。
????3.修訂談判藥品續(xù)約規(guī)則����,與工作方案一起征求社會(huì)意 見后正式發(fā)布。
??? 4.優(yōu)化完善相關(guān)材料和目錄調(diào)整信息模塊��。
??? ( 二 )申報(bào)階段( 2025 年 7 月)
??? 1.申報(bào)�����。符合條件的企業(yè)(含其他申報(bào)主體��,下同)按規(guī) 定向國(guó)家醫(yī)保局提交必要的資料�,其中需提交摘要幻燈片的 藥品�,企業(yè)在提交申報(bào)資料時(shí)同步提交摘要幻燈片。
??? 2.形式審查��。根據(jù)企業(yè)提交的資料對(duì)藥品申報(bào)資格進(jìn)行 形式審查����,審查結(jié)果分為 “通過”和 “不通過”����。對(duì)藥品摘 要幻燈片同步進(jìn)行形式審查����,不符合要求的不予采用,專家 將依據(jù)企業(yè)提交的其他材料進(jìn)行評(píng)審�����。
??? 3.公示����。對(duì)通過形式審查的藥品�����、對(duì)應(yīng)的申報(bào)目錄類別 及其相關(guān)資料(不含經(jīng)濟(jì)性信息)以及已處于非獨(dú)家狀態(tài)的 談判藥品進(jìn)行公示。
??? 4.復(fù)核��。對(duì)公示期間有關(guān)方面反饋的意見進(jìn)行梳理���,形 成形式審查最終結(jié)果����。
??? 5.公告���。對(duì)最終通過形式審查的藥品名單進(jìn)行公告,并 通過目錄調(diào)整模塊向相關(guān)企業(yè)反饋。
??? 6. 申報(bào)商保創(chuàng)新藥目錄的藥品按相應(yīng)條件進(jìn)行形式審 查��。
??? ( 三)專家評(píng)審階段( 2025 年 8-9 月)
??? 1.完善評(píng)審數(shù)據(jù)庫。根據(jù)企業(yè)申報(bào)情況�����,建立評(píng)審藥品 數(shù)據(jù)庫��,論證確定評(píng)審技術(shù)要點(diǎn)。
??? 2.專家評(píng)審����。組織藥學(xué)���、臨床、藥物經(jīng)濟(jì)學(xué)�、醫(yī)療保障���、 工傷保險(xiǎn)等方面專家開展聯(lián)合評(píng)審���。經(jīng)評(píng)審��,形成擬調(diào)入基 本目錄(包括直接/談判/競(jìng)價(jià)調(diào)入等方式)�、擬調(diào)出基本目 錄�����、擬按續(xù)約規(guī)則處理����、擬調(diào)入商保創(chuàng)新藥目錄等方面藥品 的建議名單�。 同時(shí),論證確定藥品的主規(guī)格�、參照藥品和支 付范圍,以及基本目錄凡例����、藥品名稱劑型����、目錄分類結(jié)構(gòu)���、 備注等內(nèi)容。對(duì)于簡(jiǎn)易續(xù)約的藥品���,組織專家按規(guī)則確定下 一個(gè)協(xié)議期的支付標(biāo)準(zhǔn)和支付范圍。
??? 3.擬調(diào)入商保創(chuàng)新藥目錄的藥品名單提交商保評(píng)審專 家進(jìn)行復(fù)評(píng)���,形成最終意見����。
??? 4.反饋結(jié)果���。通過目錄調(diào)整模塊向相關(guān)企業(yè)反饋結(jié)果。
??? ( 四)談判/競(jìng)價(jià)/價(jià)格協(xié)商階段( 2025 年 9-10 月)
??? 1.完善談判/競(jìng)價(jià)藥品報(bào)送材料模板����。
??? 2.根據(jù)企業(yè)意向���,組織提交相關(guān)材料�。
??? 3.開展測(cè)算評(píng)估�����。組織專家通過職工/居民醫(yī)保基金測(cè)算�����、 藥物經(jīng)濟(jì)學(xué)等方法開展評(píng)估����,提出基本目錄醫(yī)保支付標(biāo)準(zhǔn)的 評(píng)估意見���。
??? 4.加強(qiáng)與企業(yè)的信息溝通。就藥品測(cè)算評(píng)估的思路和重 點(diǎn)與企業(yè)進(jìn)行面對(duì)面溝通���,收集企業(yè)意見建議和訴求。
??? 5.開展現(xiàn)場(chǎng)談判/競(jìng)價(jià)����。根據(jù)評(píng)估意見組織開展醫(yī)保藥 品談判/競(jìng)價(jià)��,現(xiàn)場(chǎng)簽署結(jié)果確認(rèn)書。
??? 6.談判/競(jìng)價(jià)成功的藥品納入基本目錄����,并簽署談判/競(jìng) 價(jià)協(xié)議以明確相關(guān)方權(quán)利義務(wù)和管理要求����。簡(jiǎn)易續(xù)約的藥品 同期簽署續(xù)約協(xié)議���。
??? 7.參與價(jià)格協(xié)商的商保創(chuàng)新藥品按模板提交材料,專家 開展測(cè)算評(píng)估后提出協(xié)商價(jià)格的評(píng)估意見��。組織企業(yè)進(jìn)行現(xiàn) 場(chǎng)價(jià)格協(xié)商,協(xié)商成功的藥品納入商保創(chuàng)新藥目錄�,并簽署 協(xié)議。協(xié)商規(guī)則����、具體協(xié)議條款將在征求相關(guān)方意見后另行 確定���。
??? 經(jīng)專家評(píng)審建議既可以調(diào)入基本目錄也可以調(diào)入商保 創(chuàng)新藥目錄的藥品��,應(yīng)先開展基本目錄談判�����,談判失敗的進(jìn) 入價(jià)格協(xié)商環(huán)節(jié)��。
??? (五)公布結(jié)果階段( 2025 年 10-11 月)
??? 公布藥品目錄調(diào)整結(jié)果�,發(fā)布 2025 年基本目錄和商保創(chuàng)新藥目錄并組織地方做好落地執(zhí)行工作��。
??? 四�、專家構(gòu)成及職責(zé)
??? (一)基本目錄
??? 1.評(píng)審專家
??? 基本目錄評(píng)審專家分為綜合組專家和專業(yè)組專家�����。綜合 組專家由作風(fēng)正、業(yè)務(wù)強(qiáng)��、熟悉并熱心醫(yī)療保障和工傷保險(xiǎn) 事業(yè)����, 自愿參加目錄評(píng)審的藥學(xué)��、臨床�����、藥物經(jīng)濟(jì)學(xué)���、醫(yī)療 保障��、工傷保險(xiǎn)等方面的專家組成���,主要通過各省級(jí)醫(yī)保部 門�、人力資源社會(huì)保障部門和相關(guān)全國(guó)性學(xué)術(shù)團(tuán)體推薦。專 業(yè)組專家由各臨床專業(yè)的醫(yī)務(wù)人員組成���,主要通過相關(guān)全國(guó) 性學(xué)術(shù)團(tuán)體推薦�。
??? 基本目錄評(píng)審專家主要負(fù)責(zé)對(duì)納入評(píng)審范圍的藥品名 單提出評(píng)審意見,并對(duì)主規(guī)格���、參照藥品�����、支付范圍、藥品 評(píng)價(jià)與評(píng)分����,以及基本目錄凡例���、藥品名稱劑型�����、 目錄分類 結(jié)構(gòu)�����、備注等調(diào)整內(nèi)容提出意見建議。其中專業(yè)組專家主要 參與本臨床專業(yè)領(lǐng)域內(nèi)藥品的評(píng)審工作�����。
??? 2.測(cè)算專家
??? 測(cè)算專家由各省級(jí)醫(yī)保部門和相關(guān)學(xué)術(shù)團(tuán)體推薦的醫(yī) 療保障�、藥物經(jīng)濟(jì)學(xué)等方面的專家組成���,醫(yī)療保障、藥物經(jīng) 濟(jì)學(xué)專家主要負(fù)責(zé)對(duì)需談判/競(jìng)價(jià)藥品提出評(píng)估意見���。
??? 3.談判專家
??? 談判專家由醫(yī)保部門代表組成,主要負(fù)責(zé)與藥品企業(yè)進(jìn) 行現(xiàn)場(chǎng)談判/競(jìng)價(jià)����。
??? ( 二)商保創(chuàng)新藥目錄
??? 參與商保創(chuàng)新藥目錄調(diào)整的專家主要通過相關(guān)部門�����、行 業(yè)學(xué)協(xié)會(huì)����、商業(yè)保險(xiǎn)公司和省級(jí)醫(yī)保部門�、人力資源社會(huì)保 障部門推薦。
??? 1.評(píng)審專家
??? 設(shè)立商保創(chuàng)新藥目錄評(píng)審專家組,由熟悉商業(yè)保險(xiǎn)管理 方面的專家組成��,主要負(fù)責(zé)對(duì)擬調(diào)入商保創(chuàng)新藥目錄的藥品 進(jìn)行復(fù)評(píng)�����,形成最終意見�����。
??? 2.測(cè)算專家
??? 測(cè)算專家由商業(yè)保險(xiǎn)�����、藥物經(jīng)濟(jì)學(xué)專家組成���,主要負(fù)責(zé) 對(duì)相關(guān)藥品提出價(jià)格協(xié)商意見。
??? 3.價(jià)格協(xié)商專家
??? 價(jià)格協(xié)商專家由商保專家�����、醫(yī)保部門代表組成����,主要負(fù) 責(zé)與藥品企業(yè)進(jìn)行現(xiàn)場(chǎng)價(jià)格協(xié)商���。
??? 五�、監(jiān)督機(jī)制
??? (一)主動(dòng)接受監(jiān)督
??? 主動(dòng)邀請(qǐng)紀(jì)檢監(jiān)察機(jī)關(guān)對(duì)準(zhǔn)備、申報(bào)�、專家評(píng)審����、談判、 公布結(jié)果等關(guān)鍵環(huán)節(jié)監(jiān)督��。公開發(fā)布工作方案�、續(xù)約規(guī)則和 非獨(dú)家藥品競(jìng)價(jià)規(guī)則��,對(duì)通過形式審查的藥品及相關(guān)資料進(jìn) 行公示���,并對(duì)形式審查最終結(jié)果進(jìn)行公告��。加強(qiáng)與企業(yè)的溝 通����,通過召開座談會(huì)���、面對(duì)面溝通等方式建立溝通機(jī)制���,提 高目錄調(diào)整工作的透明度。在目錄調(diào)整期間�,設(shè)立專項(xiàng)電話
??? 和郵箱,接受各方面反饋的意見建議�����,主動(dòng)接受社會(huì)大眾、新聞媒體���、 醫(yī)藥企業(yè)等的監(jiān)督�����。
??? ( 二)完善內(nèi)控機(jī)制
??? 明確工作崗位和人員責(zé)任�����,制定信息保密����、利益回避、 責(zé)任追究等制度�,確保目錄調(diào)整工作公正、安全�����、有序�����。
??? ( 三)強(qiáng)化專家監(jiān)督
??? 進(jìn)一步加強(qiáng)專家管理����,明確專家遴選標(biāo)準(zhǔn)和工作要求���, 包括專家資質(zhì)�、抽取���、職責(zé)等方面,強(qiáng)化專家責(zé)任和義務(wù)����, 健全利益回避��、責(zé)任追究等制度����,加強(qiáng)專業(yè)能力培訓(xùn)����。所有 評(píng)審���、測(cè)算工作全程留痕���,確保專家獨(dú)立、公正提出意見���。 建立健全專家公正履職承諾��、保密管理��、對(duì)外宣傳等規(guī)定���, 簽訂保密協(xié)議,嚴(yán)控評(píng)審測(cè)算信息的知悉范圍���。未經(jīng)批準(zhǔn), 不得以國(guó)家藥品目錄評(píng)審�����、測(cè)算�����、談判等專家名義公開參與 活動(dòng)��。
??? ( 四)加強(qiáng)對(duì)企業(yè)行為的監(jiān)管
??? 逐步建立企業(yè)誠(chéng)信檔案,加強(qiáng)信用管理�,健全聯(lián)合懲戒 機(jī)制。對(duì)企業(yè)弄虛作假���、隱瞞信息、違法違規(guī)�, 以及其他失 信行為,查實(shí)后將視情節(jié)與目錄管理掛鉤����,實(shí)現(xiàn)聯(lián)動(dòng)���,督促 相關(guān)企業(yè)遵紀(jì)守法、誠(chéng)實(shí)守信����、公平競(jìng)爭(zhēng)���,維護(hù)醫(yī)療保障和 工傷保險(xiǎn)管理工作的嚴(yán)肅性����、規(guī)范性����、公平性���。